「寄生虫」が操る、あなたの行動: The parasite handles your behavior.
トキソプラズマ(Toxoplasma gondii)という寄生虫は、寄生した哺乳類の行動を変化させるようだ。この寄生虫は人獣共通感染症として人間にも寄生するが、その影響がどの程度なのか研究が進められている。
トキソプラズマとは何か
寄生虫の中には、その一生を特定の宿主(しゅくしゅ)に寄生し、その宿主が死ぬ前に同じ種類の宿主へ移動し、子孫を残し続けるものがいるが、発生と幼生、成体という成長段階で異なった種類の宿主の間を渡り歩くものもいる。
この過程を生活環といい、幼生時の宿主を中間宿主、成体時の宿主を終宿主という。異なった種類の宿主は、捕食非捕食の関係にあることも多い。
もし仮に、あなたが捕食関係にある違う種類の宿主を渡り歩く寄生虫だとしたら、中間宿主を終宿主に捕食してもらったほうがいい。そうすれば、まだ感染していない終宿主にも感染を広げることができるだろう。
トキソプラズマという寄生虫がいる。マラリアやトリコモナスなどと同じ病原性のある微生物の原虫で、トキソプラズマは細胞内に寄生し、有性生殖や無性生殖によって増殖する。
生活環は、主にネコ科の肉食動物が終宿主で、ネズミや鳥類などの補食者が中間宿主となる。トキソプラズマが発見されたのは1908年、ネコ科の動物を終宿主とする生活環が明らかになったのは1970年だ(※1)。
哺乳類や鳥類といった温血動物が生活環を構成し、中間宿主の間でも感染する。ほぼ世界中に分布するトキソプラズマの遺伝的多様性は低い。生活環が多岐にわたることで、短期間で急速に広がったからと考えられている。トキソプラズマの遺伝子解析をした結果、その拡散と人類の農耕牧畜の開始との関係が示唆されている。
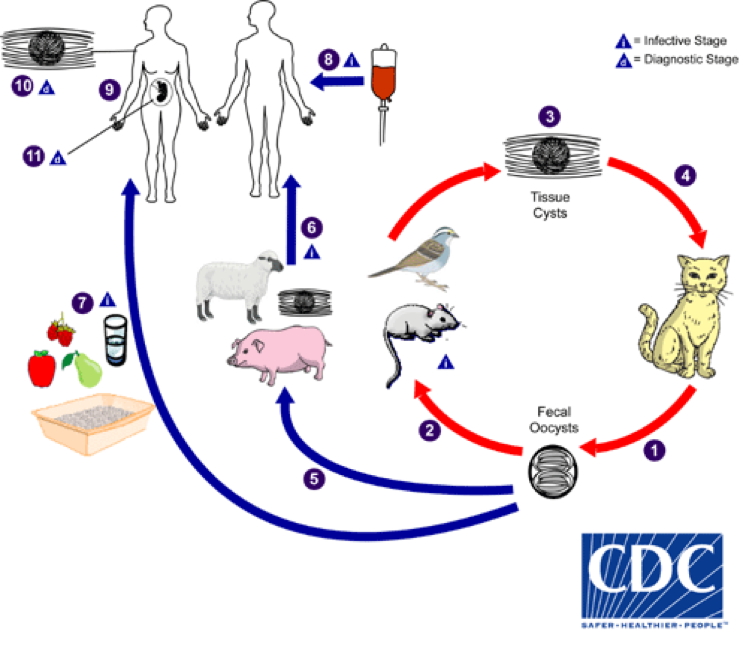
生活環を広げ、種を繁栄させるため、トキソプラズマは野良ネコなどの糞からカプセルのようなもの(オーシスト、Oocyst、接合子嚢)を放出する。そのため、ネコが糞をした公園の砂場で遊ぶ幼児などの口や目、傷口から侵入して感染することも多い。
トキソプラズマ感染に要注意
最近、妊娠中の女優がトキソプラズマに感染する危険性のあるローストビーフを食べたことがネット上で話題になった。トキソプラズマは、まれに肉の内部にまで侵入する。ブタやウシなどの家畜を含む肉食の際には、よく加熱(67℃以上)したり冷凍(-12℃以下)して駆除することが推奨されている。
トキソプラズマは、健康で免疫力が通常レベル以上の人が感染しても風邪に似た症状が出る程度でさほど重篤な症状を引き起こさないが、免疫力の落ちている病気中の人や高齢者が感染するとトキソプラズマ脳炎や肺炎などの重篤な症状を引き起こす。さらに、妊娠中の女性が感染すると、母子感染により胎児に水頭症や視力低下、脳機能障害などを引き起こす危険性も高い。
家畜、特にヒツジのトキソプラズマ症は、リンパ腫などの重篤な症状を引き起こし、母子感染により死産や子ヒツジの品質低下につながることで大きな経済的なリスクになってきた(※2)。人間を含む家畜などの排泄物が海へ流出し、現在ではクジラなどの海棲哺乳類もトキソプラズマに感染しているらしい(※3)。
健康な人がトキソプラズマに感染すると、無症状のまま原虫の保有者となることが多い。先進国の人口の約1/3、世界人口の約半分がトキソプラズマに感染したことがあると考えられ(※4)、日本の場合、妊婦を調べた研究によると感染率は約10%となっている(※5)。

寄生虫は宿主の免疫系に作用し、殺されたり体外へ排出されないようにするが、トキソプラズマも特殊なタンパク質を分泌して免疫系を欺くことが知られている。そして宿主の遺伝子コピーや細胞中のミトコンドリアの機能に関与し、炎症を起こしたり、がん化を促進したりもするようだが、そのメカニズムはまだよくわかっていない(※6)。
宿主の行動を変えるのか
ところで、あなたがもしトキソプラズマだとしたら、ネズミやスズメなどの中間宿主に感染している間、自身をネコに捕食させ、まだ感染していないネコを終宿主にしてトキソプラズマの感染を広げたくなるだろう。
トキソプラズマが宿主の行動を変えることは、50年ほど前から研究の対象になってきた。例えば、トキソプラズマに感染した中間宿主のネズミは終宿主のネコをあまり怖がらなくなり、捕食されやすくなったが、最初は感染によって単に行動が鈍ったせいと考えられた。
トキソプラズマに限らず、宿主の寿命と寄生虫の毒性による行動の鈍さ、体力の減衰は寄生虫の生活環のサイクルや再生産の割合などに微妙に影響を与える。このあたりのバランスは難しく、非捕食や毒性によって宿主の寿命が極端に短くなれば、寄生虫自身の繁殖も難しくなるだろう。
げっ歯類のラット(野生型)を使った実験では、トキソプラズマに感染したラット群のほうで嫌悪行動(新規刺激)の回避に対する反応が弱く、恐怖を感じにくい傾向があり、ネコとウサギの臭いを使った実験ではトキソプラズマに感染したラット群は危険なネコの臭いに慣れやすく、非感染群では安全なウサギの臭いへ向かう傾向があったという(※7)。
もし、こうした実験が正しければ、トキソプラズマはどうやって宿主の行動を変えているのだろう。ある仮説によれば、トキソプラズマは脳の報酬系に影響を与えているのではないかという。マウスを使った実験によれば、ドーパミンの作動が変化して野外への活動や新規探索行動が減少することがわかった(※8)。
このドーパミン仮説は人間でも考えられているが(※9)、げっ歯類はネコに補食されるので中間宿主にいるトキソプラズマとしてはネズミやラットなどを操ってネコに捕食されやすくする。
アントレプレナー精神との関係は
では、トキソプラズマは、人間の行動にも何らかの影響を与えるのだろうか。ネコ科の肉食動物は、人間と共通祖先を持つサル(霊長類)も捕食する。そうした関係があるなら、人間に寄生したトキソプラズマは、ヒョウやライオン、トラなどに人間を食べられやすくさせる可能性がある。
人間を使った実験では、トキソプラズマは男性ホルモンの一種であるテストステロンに影響を与えているようだ(※10)。トキソプラズマはドーパミンやテストステロンを増加させるが、テストステロンの多い男性は行動的攻撃的になることが知られている。
また、トキソプラズマに感染した人は、統合失調症などの精神疾患にかかりやすく、自殺の原因になる危険性があるという研究も多い(※11)。また、認知や行動を減衰させやすく自動車事故を起こす危険性も高いという。
こうしたことが次第にわかってくると、寄生虫と人間行動についての分析研究も行われるようになる(※12)。特にトキソプラズマは公衆衛生の観点からも議論され、経済や経営の分野でもその影響を評価する実験が行われるようになった(※13)。
例えば、米国のコロラド大学などの研究グループが、1495人の学生ボランティアを対象にし、トキソプラズマの感染群とそうでない群を比較した研究(※14)によれば、感染群のほうは経営学(経営管理、Major in Business)を専攻する割合が高く(約1.4倍)、マネジメントに興味があったりアントレプレナー(起業家)精神を持つ割合も高かった(約1.7倍)。また、起業セミナーへの参加者で調べたところ、自分で起業した人の割合はトキソプラズマ感染者のほうが高かった(約1.8倍)という。
トキソプラズマの感染者はドーパミンやテストステロンが高いが、だからマネジメントやアントレプレナー精神旺盛になるのだろうか。
これを逆に考えれば、こうした脳内神経物質やホルモンの高い人がトキソプラズマに感染しやすいかもしれない。自然の中で遊んだり動物と触れ合うのが好きなタイプが感染しやすいということになるが、いずれにせよトキソプラズマの感染と人間を含めた動物の行動には何らかの関係がありそうだ。
※1:W M. Hutchison, et al., “Coccidian-like Nature of Toxoplasma gondii.” BMJ, doi: https://doi.org/10.1136/bmj.1.5689.142, 142-144, 1970
※2:Jitender P. Dubey, “The History and Life Cycle of Toxoplasma gondii.” Toxoplasma Gondii, The Model Apicomplexan: Perspectives and Methods, 1-17, 2004
※3:Jitender P. Dubey, “The History of Toxoplasma gondii─The First 100 Years.” Eukeryotic Microbiology, Vol.55, Issue6, 467-475, 2008
※4:Jaroslav Flegr, et al., “Toxoplasmosis- A Global Threat. Correlation of Latent Toxoplasmosis with Specific Disease Burden in a Set of 88 Countries.” PLOS ONE, Vol.9, Issue3, 2014
※5:Makiko Sakikawa, et al., “Anti-Toxoplasma Antibody Prevalence, Primary Infection Rate, and Risk Factors in a Study of Toxoplasmosis in 4,466 Pregnant Women in Japan.” Clinical and Vaccine Immunology, Vol.19, No.3, 365-367, 2012
※6-1:Ira J. Blader, et al., “Communication between Toxoplasma gondii and its host: impact on parasite growth, development, immune evasion, and virulence.” APMIS, Vol.117(5-6), 458-476, 2009
※6-2:Ira Blader, et al., “The lytic cycle of Toxoplasma gondii: 15 years later.” The Annual Review of Microbiology,Vol.69, 463-485, 2015
※6-3:Genevieve Syn, et al., “Toxoplasma gondii Infection Is Associated with Mitochondrial Dysfunction in-Vitro.” frontiers in Cellular and Infection Microbiology, doi.org/10.3389/fcimb.2017.00512, 2017
※7-1:J P. Webster, et al., “Effect of Toxoplasma gondii upon neophobic behaviour in wild brown rats, Rattus norvegicus.” Parasitology, Vol.109, 37-43, 1994
※7-2:M Berdoy, et al., “Fatal attraction in rats infected with Toxoplasma gondii.” The Royal Society Proceedings B, VOl.267(1452), 1591-1594, 2000
※8:A Skallova, et al., “The role of dopamine in Toxoplasma-induced behavioural alterations in mice: an ethological and ethopharmacological study.” Parasitology, Vol.133, Issue5, 525-535, 2006
※9:Sule Aydin, et al., “Toxoplasma Gondii Dopamine Mechanism Related to Neuropsychiatric Diseases.” Advances in Dopamine Research, 2017
※10:Jaroslav Flegr, “Effects of Toxoplasma on Human Behavior.” Schizophrenia Bulletion, Vol.33, No.3, 757-760, 2007
※11-1:R H. Yolken, et al., “Toxoplasma and schizophrenia.” Parasite Immunology, Vol.31, Issue11, 706-715, 2009
※11-2:Fatih Yagmur, et al., “May Toxoplasma gondii increase suicide attempt-preliminary results in Turkish subjects?.” Forensic Science International, Vol.199, Issue1-3, 15-17, 2010
※11-3:Helene Lund-Sorensen, et al., “A Nationwide Cohort Study of the Association Between Hospitalization With Infection and Risk of Death by Suicide.” JAMA, Vol.73(9), 912-919, 2016
※11-4:E F. Coccaro, et al., “Toxoplasma gondii infection: relationship with aggression in psychiatric subjects.” The Journal of Clinical Psychiatry, VOl.77(3), 334-341, 2016
※11-5:Huan M. Ngo, et al., “Toxoplasma Modulates Signature Pathways of Human Epilepsy, Neurodegeneration & Cancer.” Scientific Reports, 7, Article number, 11496, 2017
※12:Robert Maseland, “Parasitical cultures? The cultural origins of institutions and development.” Journal of Economic Growth, Vol.18, Issue2, 109-136, 2013
※13:Petr Houdek, “Puppet Master: Possible Influence of the Parasite Toxoplasma Gondii on Managers and Employees.” Academy of Manegement, Vol.31, No.1, doi.org/10.5465/amp.2015.0163, 2017
※14:Stefanie K. Johnson, et al., “Risky business: linking Toxoplasma gondii infection and entrepreneurship behaviours across individuals and countries.” The Royal Sciety Proceedings of The Royal Society B, Vol.285, Issue1883, 2018

